A Complexidade da Esclerose Múltipla e a Vulnerabilidade Celular
O Ataque Autoimune e a Dificuldade de Reparo
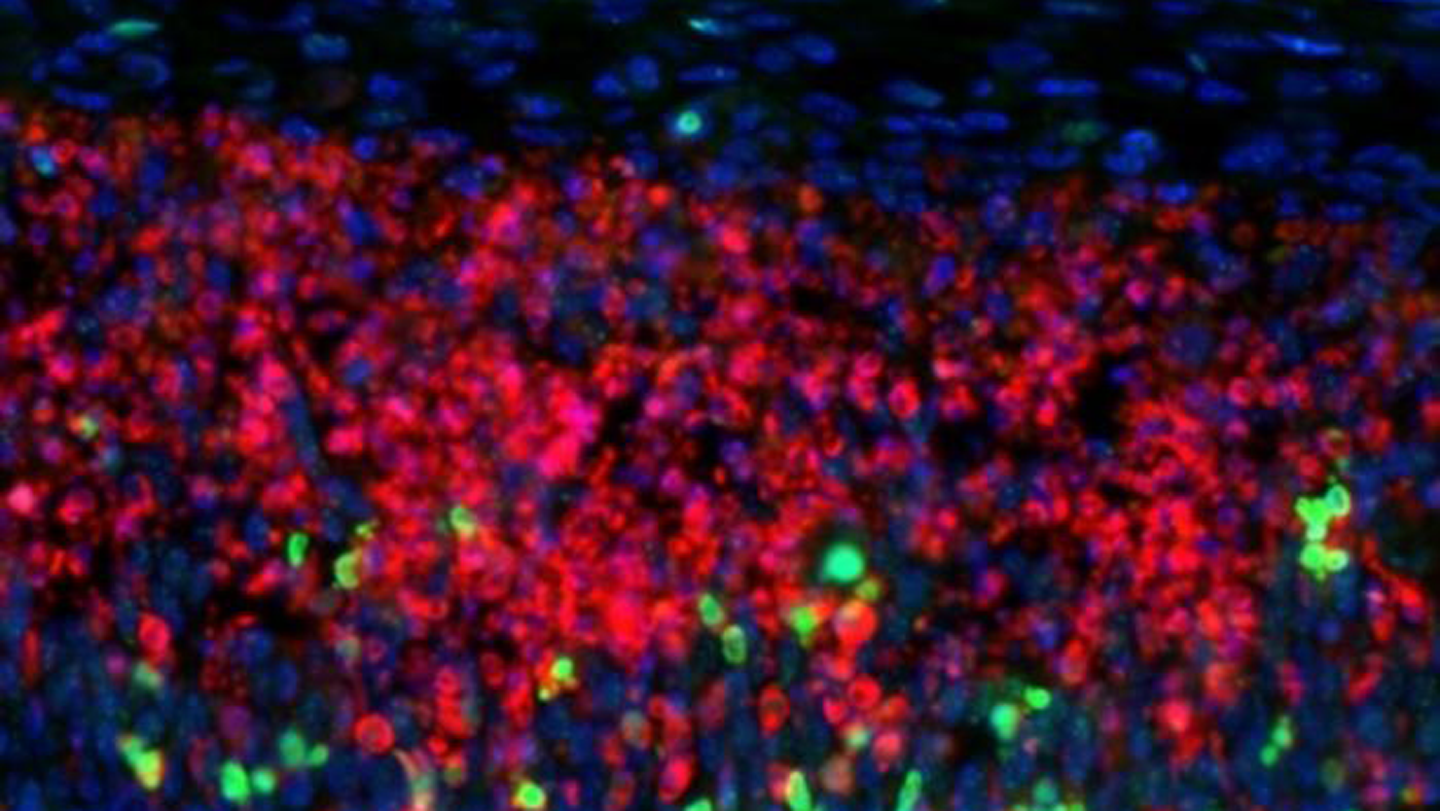
A Esclerose Múltipla é uma doença autoimune em que o sistema imunológico do corpo ataca por engano a mielina, a camada protetora que reveste os axônios dos neurônios no cérebro e na medula espinhal. Esta agressão imunológica resulta em inflamação crônica e formação de lesões (placas) que comprometem a integridade do sistema nervoso central. As células mais diretamente afetadas por este ataque são os oligodendrócitos, responsáveis pela produção e manutenção da mielina. Por muito tempo, os cientistas têm se questionado sobre a razão exata pela qual essas células são particularmente suscetíveis ao dano no ambiente inflamatório da EM, enquanto outras células cerebrais parecem resistir melhor. A perda de mielina, ou desmielinização, impede a transmissão eficiente dos impulsos nervosos, causando uma variedade de sintomas que podem incluir fadiga, fraqueza muscular, problemas de equilíbrio, dormência e dificuldades cognitivas. A natureza imprevisível e progressiva da doença torna o desenvolvimento de tratamentos desafiador, pois as terapias atuais focam principalmente em modular a resposta imunológica para reduzir a frequência e a gravidade dos surtos, mas não revertem completamente o dano existente ou previnem a neurodegeneração a longo prazo.
O ambiente inflamatório crônico na EM não é apenas um catalisador para o ataque imunológico, mas também um gerador de estresse oxidativo significativo. As células imunes ativadas liberam uma série de moléculas pró-inflamatórias, incluindo radicais livres e espécies reativas de oxigênio (ROS). Esses compostos são altamente reativos e podem causar danos substanciais a componentes celulares essenciais, como proteínas, lipídios e, crucialmente, o DNA. A capacidade de uma célula de reparar o DNA danificado é vital para sua sobrevivência e função. Se o dano ao DNA se acumular sem reparo adequado, isso pode levar à morte celular, comprometendo ainda mais a capacidade do cérebro de se reparar ou funcionar. Compreender como os oligodendrócitos lidam ou falham em lidar com esse estresse inflamatório e o consequente dano genético é fundamental para desvendar os mecanismos subjacentes à sua vulnerabilidade na EM e, potencialmente, identificar novos alvos terapêuticos que possam proteger essas células e promover a remielinização.
A Descoberta: Dano ao DNA Supera Capacidade de Reparo
Entendendo a Cascata de Inflamação e Dano Genético
A recente pesquisa inovadora aponta para um mecanismo fundamental que explica a vulnerabilidade dos oligodendrócitos na Esclerose Múltipla: a inflamação crônica no cérebro dos pacientes com EM gera níveis tão elevados de dano ao DNA que os sistemas de reparo celular intrínsecos dos oligodendrócitos são simplesmente sobrecarregados. Em condições normais, as células possuem mecanismos robustos para detectar e reparar danos ao DNA, garantindo a integridade do genoma. No entanto, o microambiente hostil criado pela EM, com sua cascata contínua de moléculas inflamatórias e oxidantes, impõe um desafio insuperável. Estudos realizados tanto em culturas de células cerebrais humanas quanto em modelos animais de EM revelaram que, sob o estresse inflamatório, os oligodendrócitos acumulam danos significativos no DNA que não conseguem ser corrigidos a tempo ou de forma eficaz. Esse desequilíbrio entre dano e reparo é o cerne da vulnerabilidade celular.
A suscetibilidade particular dos oligodendrócitos a esse fenômeno pode estar ligada a várias características específicas. Primeiro, essas células são metabolicamente muito ativas devido à demanda energética para produzir e manter a mielina, tornando-as mais sensíveis ao estresse oxidativo. Segundo, pode haver diferenças inerentes na eficiência de seus sistemas de reparo de DNA em comparação com outros tipos de células cerebrais, ou eles podem expressar enzimas de reparo em níveis insuficientes para combater o ataque implacável. Quando o dano ao DNA atinge um ponto crítico, a célula pode iniciar a apoptose (morte celular programada) ou entrar em um estado de senescência, perdendo sua capacidade funcional. A perda contínua de oligodendrócitos, impulsionada por esse ciclo vicioso de inflamação e dano ao DNA não reparado, perpetua a desmielinização e impede a remielinização, contribuindo para a progressão da doença e a acumulação de incapacidade neurológica. A identificação desta falha no equilíbrio entre dano e reparo genético oferece uma nova e poderosa lente através da qual se pode entender a patogênese da EM e, mais importante, desenvolver estratégias terapêuticas inovadoras.
Novas Perspectivas para Tratamentos e a Próxima Fronteira na Pesquisa
A descoberta de que o dano ao DNA induzido pela inflamação supera a capacidade de reparo das células cerebrais em Esclerose Múltipla abre caminho para uma era de tratamentos mais específicos e eficazes. Até agora, muitas das terapias para EM têm focado na modulação da resposta imune, buscando reduzir a inflamação sistêmica. Contudo, esta nova compreensão sugere que o foco pode ser expandido para incluir estratégias que visem diretamente a proteção celular e a otimização dos mecanismos de reparo. Uma linha de pesquisa promissora seria o desenvolvimento de fármacos capazes de potencializar a capacidade inata dos oligodendrócitos de reparar seu DNA, tornando-os mais resistentes aos efeitos deletérios da inflamação. Isso poderia envolver a ativação de vias de reparo específicas ou o aumento da expressão de enzimas de reparo.
Além disso, o controle mais eficiente do estresse oxidativo no microambiente cerebral se torna ainda mais crítico. Antioxidantes mais potentes ou agentes que inibam a produção de espécies reativas de oxigênio por células imunes poderiam desempenhar um papel fundamental na redução do dano inicial ao DNA. Outra abordagem fascinante seria o desenvolvimento de terapias neuroprotetoras que não apenas evitem a morte dos oligodendrócitos existentes, mas também promovam a diferenciação e maturação de novas células produtoras de mielina a partir de células-tronco, facilitando a remielinização e, potencialmente, a recuperação da função neurológica. A translação desta pesquisa básica para a prática clínica exigirá estudos pré-clínicos rigorosos e, eventualmente, ensaios clínicos em humanos para avaliar a segurança e eficácia de novas abordagens terapêuticas. Este avanço representa uma luz de esperança para milhões de pessoas que vivem com Esclerose Múltipla em todo o mundo, sinalizando uma futura geração de tratamentos que não apenas mitigam os sintomas, mas também abordam a raiz da degeneração celular, transformando a paisagem da gestão da doença.
Fonte: https://www.sciencenews.org